Branchenhintergrund und Herausforderungen
Hohe Sterilitätsanforderungen:
Bei der Arzneimittelzubereitung muss eine mikrobielle und partikelförmige Kontamination vermieden werden.
Hoher Compliance-Druck:
Strenge Standards wie FDA, EU GMP und USP <797> müssen erfüllt werden.
Schwierige Erweiterung:
Die bestehenden Einrichtungen können den Bedürfnissen des Unternehmenswachstums nur schwer gerecht werden.

Warum benötigen Apotheken USP-konforme Reinräume?
Apotheken in den Vereinigten Staaten sind verpflichtet, die USP- und USP-Standards für die Herstellung steriler und gefährlicher Arzneimittel einzuhalten. Diese Vorschriften dienen dem Schutz von Patienten und medizinischem Fachpersonal, der Minimierung von Kontaminationsrisiken und der Kontrolle des Umgangs mit Gefahrstoffen.
Häufige Herausforderungen in Apotheken:
- Aufrechterhaltung von ISO-klassifizierten Umgebungen
- Vermeidung von Kreuzkontaminationen zwischen gefährlichen und ungefährlichen Bereichen
- Steuerung von Luftdruckdifferenzen und Luftstrom
- Sicherstellung ordnungsgemäßer Schutzkleidungs- und Materialtransferverfahren.
Übersicht der Reinraumzonierung
Ein USP-konformer Reinraum umfasst typischerweise die folgenden Funktionsbereiche:
-
Umkleidebereich zum Anlegen persönlicher Schutzausrüstung (PSA)
-
Deutlich gekennzeichnete Schmutz- und Sauberzonen auf dem Boden
-
Handwaschbecken mindestens 1 Meter von der Eingangstür entfernt
-
Augendusche in der Nähe von Gefahrenbereichen
-
Dient als Übergangszone zu Nicht-HD- und HD-Räumen
-
Positiver Druck im Vergleich zum Vorraum
-
Ausgestattet mit Laminar-Airflow-Werkbänken (LAFWs)
-
HEPA-gefilterte Luft; unterstützt die sterile Zubereitung von Nicht-HD-Arzneimitteln
-
Unterdruck im Vergleich zu angrenzenden Räumen
-
Die Abluft wird nicht umgewälzt und nach außen abgeleitet.
-
Enthält biologische Sicherheitswerkbänke (BSCs) der Klasse II Typ B2
-
Unterstützt sowohl HD- als auch Nicht-HD-Räume
-
Stabile Temperatur- und Feuchtigkeitsumgebung
-
Beherbergt Lüftungsanlagen und zugehörige Ausrüstung
-
Zur getrennten Lagerung von gefährlichen Arzneimitteln
-
Zugang vom Vorraum in der gleichen Luftstromrichtung
Ablauf- und Layoutprinzipien
neutral/ante → Reine Bereiche → Verbandbereich → Puffer → Steriler Vorbereitungsbereich
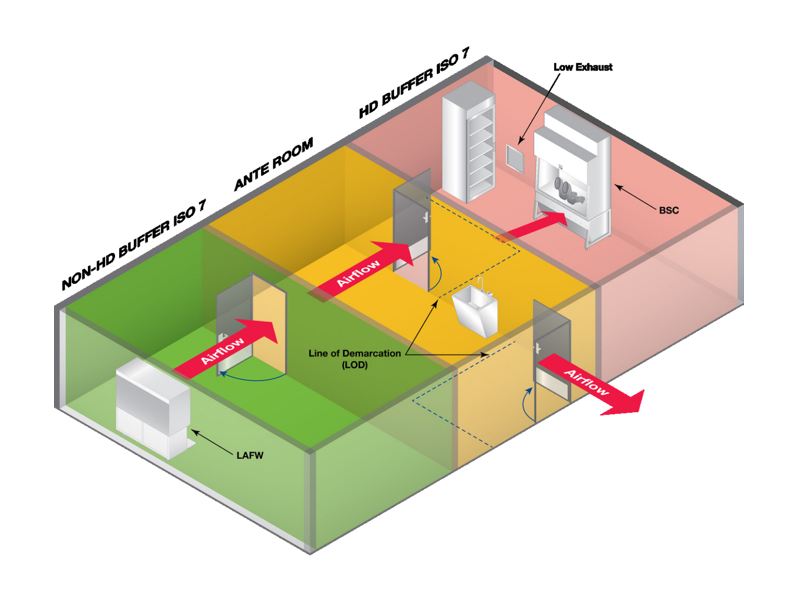
Was ist ein GMP-Reinraum?
Im pharmazeutischen Kontext bezeichnet ein Reinraum einen Raum, der die in den GMP-Sterilitätsvorgaben definierten GMP-Spezifikationen erfüllt (d. h. Anhang 1 der EU- und PIC/S-GMP-Leitlinien sowie weitere von den lokalen Gesundheitsbehörden geforderte Normen und Richtlinien). Die Umwandlung eines normalen Raums in einen Reinraum erfordert eine Kombination aus technischen, fertigungstechnischen, ausstattungstechnischen und betrieblichen Kontrollmaßnahmen (Kontrollstrategien).
Gemäß den einschlägigen Standards der FDA gelten in der pharmazeutischen Industrie strenge und präzise Vorschriften für Arzneimittelhersteller. Die Gute Herstellungspraxis (GMP) für die Herstellung steriler Arzneimittel soll sicherstellen, dass diese sicher sind und die deklarierten Inhaltsstoffe in der angegebenen Menge enthalten. Diese Standards zielen darauf ab, das Risiko mikrobieller, partikulärer und pyrogener Kontaminationen zu minimieren. Diese Regelung, auch bekannt als aktuelle Gute Herstellungspraxis (cGMP), umfasst Produktionsprozesse, Qualitätskontrolle, Verpackung, Personal und GMP-konforme Anlagen.

Anpassung der GMP-Standards an pharmazeutische Produktionsprozesse

- Note A:Eine abgegrenzte Zone für Hochrisikovorgänge wie aseptische Abfüllung und sterile Verbindungen. Typischerweise wird dies durch eine Laminar-Flow-Box (LAF-Box) oder einen Isolator in einem Reinraum der Klasse B realisiert.
- Note B:Die Hintergrundumgebung für eine Klasse-A-Zone bei aseptischer Vorbereitung und Abfüllung.
- Note C:Wird zur Durchführung weniger kritischer Verfahrensschritte bei der Herstellung steriler Produkte oder für die Endsterilisation eingesetzt.
- Note D:Ein Vorbereitungsbereich für weniger kritische Arbeitsschritte, wie z. B. das Waschen von Geräten oder das Hantieren mit Bauteilen vor der Sterilisation.
Grundprinzipien der konformen Reinraumgestaltung
Ein konformes Design integriert mehrere Elemente zu einer ganzheitlichen Strategie zur Kontaminationskontrolle.
- Luftstrom- und DruckkaskadenDas mit Abstand wichtigste Gestaltungselement ist die Kontrolle über die Luft.
- Luftstrom:In Reinraumzonen der Klasse A wird eine unidirektionale (laminare) Strömung eingesetzt, um Partikel vom kritischen Prozess abzutransportieren. In Räumen niedrigerer Reinraumklassen wird eine nicht-unidirektionale (turbulente) Strömung verwendet, um Verunreinigungen zu verdünnen und zu entfernen.
- Druckdifferenzen:Es wird ein kaskadiertes Überdrucksystem aufrechterhalten, wobei der höchste Druck im kritischsten Bereich herrscht. Dadurch wird sichergestellt, dass die Luft von saubereren zu weniger sauberen Bereichen strömt und das Eindringen von Schadstoffen verhindert wird. Die typische Druckdifferenz zwischen benachbarten Räumen beträgt 10–15 Pascal.
Layout, Fluss und OberflächenDie räumliche Anordnung muss logische Arbeitsabläufe für Personal, Material und Abfall unterstützen, um Verwechslungen und Kreuzkontaminationen zu vermeiden.
- Materialien:Alle Oberflächen müssen glatt, abriebfest, porenfrei und beständig gegen wiederholte Reinigungs- und Desinfektionsmittel sein. Gängige Materialien sind epoxidbeschichtete Böden, uPVC- oder HPL-Wandpaneele und integrierte Hohlkehlen zwischen Wänden und Böden.
- Layout:Die Konstruktion muss separate Schleusen für Personal (Umkleideräume) und Material (Materialschleusen - MALs) vorsehen, um Pufferzonen zwischen verschiedenen Klassifizierungszonen zu schaffen.

Kritische technische Systeme: Heizung, Lüftung und Klimaanlage sowie Überwachung

- Pharmazeutische HLK-SystemeDie Heizungs-, Lüftungs- und Klimaanlage (HLK-Anlage) ist das Herzstück des Reinraums. Sie sorgt für die Zufuhr der richtigen Luftmenge und -qualität, die Kontrolle von Temperatur und Luftfeuchtigkeit sowie die Aufrechterhaltung der Druckkaskade. Zu den wichtigsten Komponenten gehören spezielle Lüftungsgeräte, mehrstufige Filteranlagen (einschließlich HEPA-/ULPA-Endfilter) und hochentwickelte Steuerungssysteme.
Umweltüberwachungssysteme (UMS)Ein moderner Reinraum benötigt ein kontinuierliches oder häufiges Überwachungssystem, um Echtzeitdaten über seinen Kontrollzustand zu liefern. Dies umfasst:
- Nicht funktionsfähige Partikelzähler
- Lebende (mikrobielle) Luftprobenahmegeräte
- Differenzdruckmessgeräte
- Temperatur- und Feuchtigkeitssensoren
Unsere GMP-konformen Reinraumlösungen für Apotheken

Kundenspezifisches Design:
Reinraumlayout und -funktionen können an die Bedürfnisse der Apotheke angepasst werden.
Konformitätsgarantie:
Reinräume entsprechen den Standards der FDA, EU GMP und USP <797>.
Flexible Erweiterung:
Das modulare Design ermöglicht spätere Erweiterungen und Aufrüstungen.
